2 × Taq PCR MasterMix Ⅱ
Caracteristici
■ Eficiență ridicată a amplificării: fragmente de ADN de diferite dimensiuni (mai mici de 5 kb) și surse pot fi amplificate eficient.
■ Sensibilitate ridicată: până la 10 pg de fragmente țintă pot fi amplificate din șabloane genomice.
■ Rezistență ridicată la stres: Pentru șabloanele cu conținut ridicat de impurități, cum ar fi șablonul extras brut / cultura bacteriană, fragmentul țintă poate fi ușor amplificat. Activitatea polimerazei nu va fi afectată de înghețarea și dezghețarea repetate.
■ Convenabil pentru aplicații: sistemul de reacție a fost pregătit ușor și rapid. Fragmentul amplificat conține capătul de 3 'dA-overhang, care este convenabil pentru clonarea TA.
Specificație
Tip: Taq ADN polimerază
Probă: Șablon purificat / extras brut / cultură bacteriană
Șablon: > 10 pg
Dimensiunea fragmentului: <5 kb
Aplicații: Amplificarea PCR a fragmentelor de ADN, marcarea ADN-ului, extinderea primerului, determinarea secvenței, detectarea genelor la scară largă, experimente PCR semicantitative, detectarea urmelor de ADN etc.
Toate produsele pot fi personalizate pentru ODM / OEM. Pentru detalii,vă rugăm să faceți clic pe Serviciu personalizat (ODM / OEM)
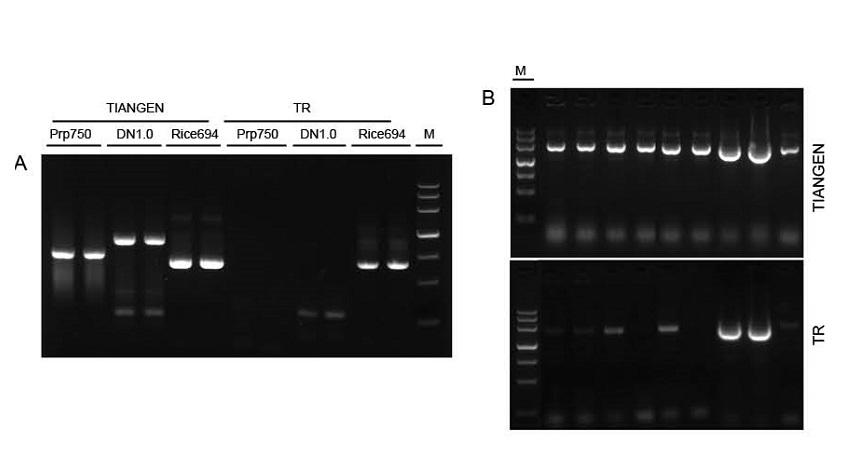 |
Figura 1. Șabloanele din surse diferite au fost amplificate de TIANGEN Taq MasterMix II și respectiv de Taq Mix comun de la furnizorul TR pentru a detecta rezistența la stres a reactivilor. Rezultatele arată că produsele TIANGEN pot amplifica fragmentele țintă din șabloane genomice brute și cultura bacteriană, iar rezistența la stres este mai bună decât cea a furnizorului TR. A: Șablon genomic brut extras de TIANGEN TIANcombi DNA Lyse & Det PCR Kit. Prp / DN: Extracția brută și detectarea probelor de sânge uman. Orez: Extracția brută și detectarea probelor de orez. B: Colonia PCR. Fragmentul PCR este de 700 bp. M: TIANGEN Marker III |
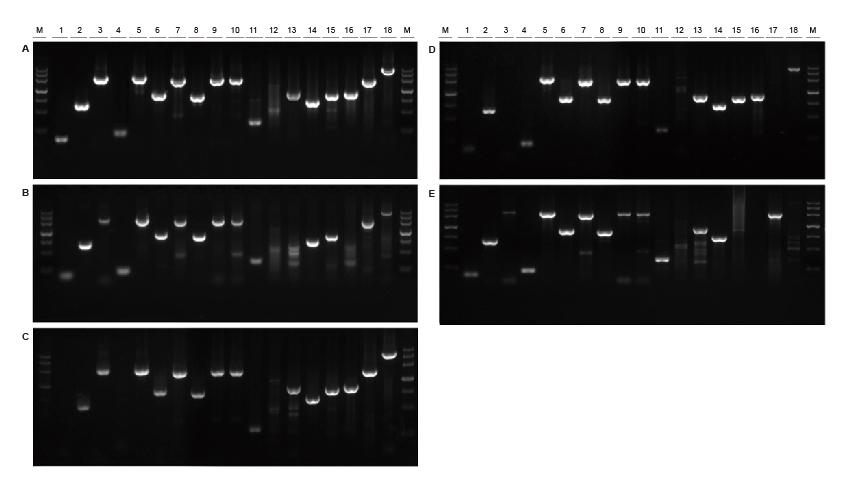 |
Bună universalitate pentru șabloane din surse diferite și cu lungimi diferite Figura 2. Fragmente de diferite surse și lungimi au fost amplificate folosind TIANGEN Taq MasterMix II (A) și obișnuit Taq Amestec de furnizorul de cunoștințe tehnice (B), furnizorul TR (C), furnizorul V (D) și respectiv furnizorul G (E). Rezultatele arată că performanța cuprinzătoare a produselor TIANGEN este cea mai bună în ceea ce privește capacitatea de amplificare, specificitatea și universalitatea. M: TIANGEN Marker III1: Șablon ADN genomic de soia (120 bp); 2-3: șablon ADN genomic de orez (694 pb, 2258 pb); 4: Șablon ADN genomic de bumbac (200 pb); 5: Escherichia coli model ADN genomic (2298 pb); 6-7: Șablon ADN al genomului șoarecelui (1 kb, 2 kb); 8-10: Șablon ADN genomic de șobolan (1 kb, 2 kb, 2080 bp); 11-18: șablon de ADN al genomului uman (300 bp, 448 bp (GC%: 74,8%), 1100 bp, 750 bp, 1000 bp, 1090 bp (GC%: 70,4%), 2 kb, 4 kb) |
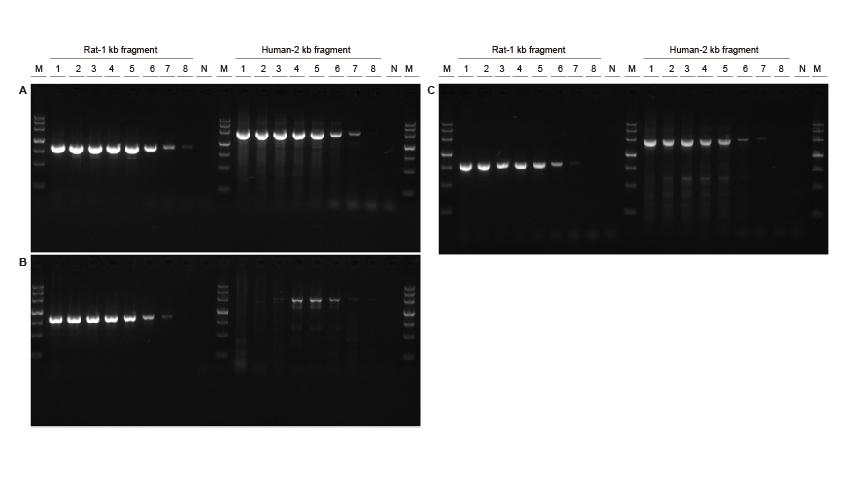 |
Sensibilitate crescută Figura 3. Concentrații diferite de fragmente de ADN de șobolan și uman au fost amplificate folosind TIANGEN Taq MasterMix II (A), obișnuit Taq Amestec de furnizorul V (B) și respectiv furnizorul TK (C), pentru a detecta sensibilitatea amplificării. Rezultatele arată că produsul TIANGEN ar putea amplifica fragmentul țintă din șablonul genomului până la 0,01 ng, iar sensibilitatea acestuia este mai bună decât cea a produselor de la furnizorul V și TK.M: TIANGEN Marker III, N: NTCTemplare de intrare 1-8 : 200 ng, 100 ng, 50 ng, 20 ng, 10 ng, 1 ng, 0,1 ng, 0,01 ng. |
Șablon A-1
■ Șablonul conține impurități proteice sau inhibitori Taq etc. —— Purificați șablonul ADN, eliminați impuritățile proteice sau extrageți ADN șablon cu kituri de purificare.
■ Denaturarea șablonului nu este completă - Creșteți corespunzător temperatura de denaturare și prelungiți timpul de denaturare.
■ Degradarea șablonului - Pregătiți din nou șablonul.
A-2 Grund
■ Calitatea slabă a primerilor —— Re-sintetizați primerul.
■ Degradarea primerului ——Aliquot primerii cu concentrație mare în volum mic pentru conservare. Evitați înghețarea și dezghețarea multiplă sau crioconservarea pe termen lung de 4 ° C.
■ Proiectarea necorespunzătoare a grundurilor (de exemplu, lungimea grundului nu este suficientă, dimerul format între grunduri etc.) -Grunduri de reproiectare (evita formarea dimerului grundului și a structurii secundare)
A-3 Mg2+concentraţie
■ Mg2+ concentrația este prea mică ——Măriți în mod corespunzător Mg2+ concentrație: Optimizați Mg2+ concentrație printr-o serie de reacții de la 1 mM la 3 mM cu un interval de 0,5 mM pentru a determina Mg optim2+ concentrația pentru fiecare șablon și grund.
A-4 Temperatura de recoacere
■ Temperatura ridicată de recoacere afectează legarea grundului și șablonului. —— Reduceți temperatura de recoacere și optimizați starea cu un gradient de 2 ° C.
A-5 Timp de prelungire
■ Timp scurt de prelungire —— Măriți timpul de prelungire.
Fenomene: eșantioanele negative arată, de asemenea, benzile secvenței țintă.
A-1 Contaminarea PCR
■ Contaminarea încrucișată a secvenței țintă sau a produselor de amplificare —— Nu pipetați cu atenție proba care conține secvența țintă în eșantionul negativ sau vărsați-le din tubul centrifugii. Reactivii sau echipamentele ar trebui să fie autoclavizate pentru a elimina acizii nucleici existenți, iar existența contaminării ar trebui determinată prin experimente de control negativ.
■ Contaminarea reactivului ——Alocați reactivii și depozitați la temperatură scăzută.
A-2 Primer
■ Mg2+ concentrația este prea mică ——Măriți în mod corespunzător Mg2+ concentrație: Optimizați Mg2+ concentrație printr-o serie de reacții de la 1 mM la 3 mM cu un interval de 0,5 mM pentru a determina Mg optim2+ concentrația pentru fiecare șablon și grund.
■ Proiectarea necorespunzătoare a primerului, iar secvența țintă are omologie cu secvența non-țintă. —— Grunduri de reproiectare.
Fenomene: benzile de amplificare PCR sunt incompatibile cu dimensiunea așteptată, fie mare, fie mică, sau uneori apar ambele benzi de amplificare specifice și benzi de amplificare nespecifice.
A-1 Primer
■ Specificitate slabă a primerului
—— Grund pentru reproiectare.
■ Concentrația grundului este prea mare ——Măriți în mod corespunzător temperatura de denaturare și prelungiți timpul de denaturare.
A-2 Mg2+ concentraţie
■ Mg2+ concentrația este prea mare —— Reduceți în mod corespunzător concentrația de Mg2 +: Optimizați Mg2+ concentrație printr-o serie de reacții de la 1 mM la 3 mM cu un interval de 0,5 mM pentru a determina Mg optim2+ concentrația pentru fiecare șablon și grund.
A-3 Polimerază termostabilă
■ Cantitate excesivă de enzime —— Reduceți cantitatea enzimatică în mod adecvat la intervale de 0,5 U.
A-4 Temperatura de recoacere
■ Temperatura de recoacere este prea scăzută ——Măriți corespunzător temperatura de recoacere sau adoptați metoda de recoacere în două etape
A-5 cicluri PCR
■ Prea multe cicluri PCR —— Reduceți numărul de cicluri PCR.
A-1 Primer—— Specificitate slabă —— Re-proiectați grundul, schimbați poziția și lungimea grundului pentru a spori specificitatea acestuia; sau efectuați PCR imbricat.
A-2 Șablon ADN
—— Șablonul nu este pur —— Purificați șablonul sau extrageți ADN cu kituri de purificare.
A-3 Mg2+ concentraţie
——Mg2+ concentrația este prea mare —— Reduceți în mod corespunzător Mg2+ concentrație: Optimizați Mg2+ concentrație printr-o serie de reacții de la 1 mM la 3 mM cu un interval de 0,5 mM pentru a determina Mg optim2+ concentrația pentru fiecare șablon și grund.
A-4 dNTP
——Concentrația de dNTP este prea mare —— Reduceți în mod corespunzător concentrația de dNTP
A-5 Temperatura de recoacere
——Temperatura prea scăzută de recoacere ——Măriți corespunzător temperatura de recoacere
A-6 Cicluri
——Prea multe cicluri ——Optimizați numărul ciclului

Primul pas este alegerea polimerazei adecvate. Polimeraza Taq regulată nu poate fi corectată din cauza lipsei activității de exonuclează 3'-5 'și nepotrivirea va reduce considerabil eficiența extensiei fragmentelor. Prin urmare, polimeraza Taq obișnuită nu poate amplifica în mod eficient fragmente țintă mai mari de 5 kb. Taq polimeraza cu modificări speciale sau altă polimerază de înaltă fidelitate ar trebui selectată pentru a îmbunătăți eficiența extensiei și pentru a satisface nevoile de amplificare a fragmentelor lungi. În plus, amplificarea fragmentelor lungi necesită, de asemenea, ajustarea corespunzătoare a designului primerului, timpul de denaturare, timpul de extindere, pH-ul tampon etc. De obicei, primerii cu 18-24 bp pot duce la un randament mai bun. Pentru a preveni deteriorarea șablonului, timpul de denaturare la 94 ° C ar trebui redus la 30 sec sau mai puțin pe ciclu, iar timpul de creștere a temperaturii la 94 ° C înainte de amplificare ar trebui să fie mai mic de 1 min. Mai mult, setarea temperaturii de extindere la aproximativ 68 ° C și proiectarea timpului de extindere în funcție de rata de 1 kb / min poate asigura o amplificare eficientă a fragmentelor lungi.
Rata de eroare a amplificării PCR poate fi redusă utilizând diverse ADN polimeraze cu fidelitate ridicată. Dintre toate ADN polimerazele Taq găsite până acum, enzima Pfu are cea mai mică rată de eroare și cea mai mare fidelitate (vezi tabelul atașat). În plus față de selecția enzimei, cercetătorii pot reduce în continuare rata de mutație a PCR prin optimizarea condițiilor de reacție, inclusiv optimizarea compoziției tampon, concentrația polimerazei termostabile și optimizarea numărului ciclului PCR.
Categorii de produse
DE CE NE ALEGE
De la înființare, fabrica noastră dezvoltă produse de primă clasă mondială, respectând principiul
de calitate mai întâi. Produsele noastre au câștigat o reputație excelentă în industrie și o valoare de încredere în rândul clienților noi și vechi ..








